Équipe Philippe MARIN
Neuroprotéomique et signalisation des pathologies cérébrales
Projet Contrôle de la température et du rythme circadien dans la physiopathologie de la maladie d’Alzheimer
RESPONSABLE

Personnel IGF impliqué
Laurent GIVALOIS
CRCN CNRS
Sylvie CLAEYSEN
CRHC Inserm
Philippe MARIN
DRCE CNRS
Carine BÉCAMEL
PU UM
Charleine ZUSSY
Chercheur CDD UM
Magalie MATHIAS
IE CDD UM
Nicolas MARCHI
CRHC CNRS

La maladie d’Alzheimer (MA) est une maladie neurodégénérative progressive définie par des plaques de β-amyloïde (Aβ) et des enchevêtrements de tau dont la propagation corrèle avec le déclin cognitif. Le sommeil et la MA interagissent bidirectionnellement : les perturbations du sommeil élèvent les niveaux d’Aβ et de tau et en accélèrent la diffusion. En conditions physiologiques, le cycle veille–sommeil (CVS) régule les concentrations d’Aβ et de tau via la sécrétion, la recapture neuronale et la clairance glymphatique. De plus, les variations de la température corporelle (TC) au cours du CVS sont atténuées dans la MA et associées à une aggravation de la pathologie. Nos données expérimentales indiquent que les fluctuations de TC contrôlent la protéostase de tau : une TC plus basse durant le sommeil augmente la phosphorylation de tau et réduit sa sécrétion. Ce projet vise à tester comment la TC module la recapture, la clairance et la propagation d’Aβ/tau, et évaluera la thérapie thermale comme approche complémentaire non pharmacologique.
Nous émettons l’hypothèse que les variations circadiennes de température corporelle (TC) régulent la sécrétion, la recapture et la clairance d’Aβ et de tau. Ce projet vise à élucider le cercle vicieux reliant les déficits de thermorégulation, les troubles du sommeil et la dysfonction glymphatique à la propagation d’Aβ et de tau. Comprendre ces liens permettra de proposer des stratégies thérapeutiques innovantes. Les objectifs spécifiques sont :
- Objectif 1. Déterminer si les variations de TC au cours du cycle veille–sommeil régulent la recapture de tau.
Définir comment les fluctuations de TC (35–38 °C) modulent la recapture neuronale et la propagation cellule-à-cellule de tau, avec un focus sur le rôle de Syndecan-3 (SDC3). - Objectif 2. Déterminer si les variations de TC au cours du cycle veille–sommeil régulent la propagation d’Aβ.
Établir comment la TC module la production et la recapture d’Aβ (rôle de SDC3) et sa propagation, via des approches in vitro, in vivo et des analyses cliniques corrélatives. - Objectif 3. Tester si l’inhibition génétique de SDC3 empêche la propagation des pathologies amyloïde et tau dans des modèles murins de MA soumis à la privation de sommeil.
Évaluer si l’inhibition de SDC3 (KO/siRNA) bloque la sécrétion, la recapture et la propagation de tau/Aβ et améliore la cognition après privation de sommeil chronique ; quantifier tau/Aβ dans le LCI/LCR (ISF/CSF) et la charge pathologique. - Objectif 4. Déterminer si la TC influence la clairance glymphatique d’Aβ et de tau.
Définir comment la TC module la clairance glymphatique de tau/Aβ (expression/polarisation d’AQP4 ; microdialyse des flux ISF↔LCR/plasma). Évaluer la thérapie thermale contrôlée comme stratégie non pharmacologique et analyser les effets de l’inhibition d’AQP4 sur le sommeil, la thermorégulation et la pathologie.
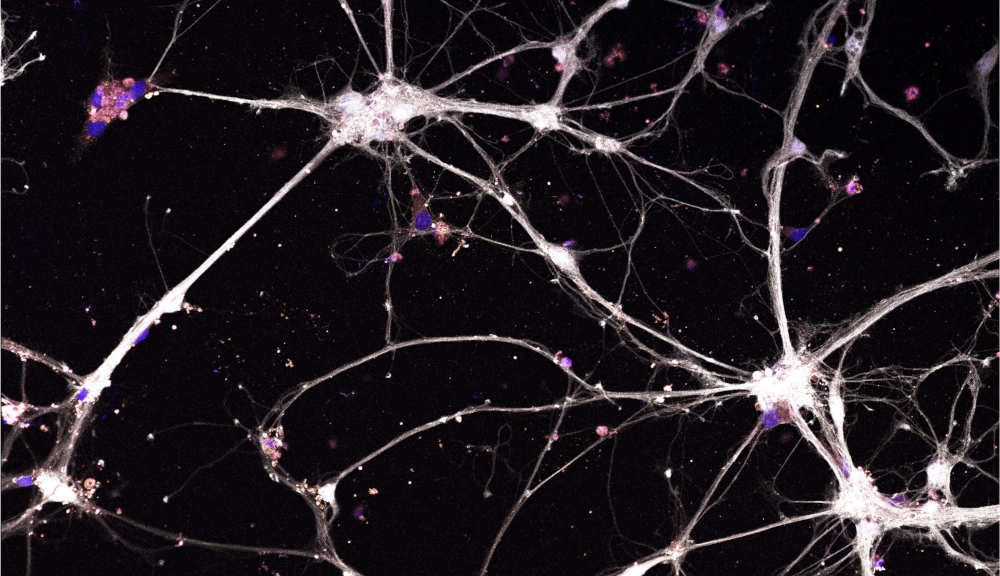
Image de microscopie confocale représentant des neurones corticaux primaires de souris marqués pour la protéine fluorescente rouge (RFP, en blanc), le DAPI (en bleu) et la syndécan-3 (en violet). Les cellules ont été exposées à 38 °C pendant 72 heures. Grossissement 20×.
Principales publications
• Canet G., et al. (2025) J Clin Invest, 135, e182931.
• Canet G., et al. (2025) Brain, 148, 9-11.
• Canet G., et al. (2023) Exp Neurobiol, 32, 423-440.
• Guisle I., et al. (2022) Neurobiol Aging, 113,118-130.
Financements
• 2026-2029 Association France Alzheimer – ARCP
Collaborations
• Emmanuel Planel (Quebec, QC, Canada)
• Esther M Blessing (New York, NY, USA)
• Brendan P Lucey (St. Louis, MO, USA)


