Le récepteur GABAB a été le premier récepteur hétérodimérique obligatoire identifié en 1998. Il est composé de deux sous-unités similaires codées par deux gènes distincts : GABAB1 et GABAB2. L’analyse structurale a révélé que chaque sous-unité joue un rôle spécifique : la sous-unité GABAB1 contient le site de liaison de l’agoniste, tandis que la sous-unité GABAB2 est responsable de l’activation de la protéine G. La manière dont la liaison d’un ligand à une sous-unité peut entraîner l’activation de la sous-unité associée a fait l’objet de nombreuses études menées par le groupe de Jean-Philippe Pin à l’IGF. Ces travaux ont conduit à l’hypothèse selon laquelle la liaison d’un agoniste au domaine de liaison de GABAB1 induit sa fermeture, entraînant un mouvement relatif entre les sous-unités et conduisant à une nouvelle interface active de leur domaine membranaire impliquant l’hélice transmembranaire 6. Cette hypothèse a été formellement validée par la détermination de la structure par cryo-microscopie électronique du récepteur GABAB dans son état basal et son état actif, avec et sans la protéine G associée. Ces études structurales ont révélé un mode d’activation de la protéine G très différent de celui utilisé par la plupart des autres récepteurs couplés aux protéines G (RCPG), sans mouvement de TM6, et une interaction avec la protéine G du côté de la sous-unité GABAB2, impliquant les boucles intracellulaires. Ce mécanisme a ensuite été observé pour tous les RCPG de classe C.
Le récepteur GABAB est plus complexe sur le plan structurel que la plupart des autres RCPG. Le groupe animé par Jean-Philippe Pin a montré grâce au développement de la technologie SNAP htrf en collaboration avec Revvity, que i) le récepteur GABAB pouvait s’associer en entités plus grandes, composées d’au moins deux hétérodimères GABAB, associés via la sous-unité GABAB1 et ii) ces complexes sont stables à la surface cellulaire et conduisent à une allostérie négative entre les hétérodimères car un seul peut se lier à un ligand et transmettre le signal6. Plusieurs évidences soutiennent la présence de tétramères GABAB dans le cerveau, notamment l’analyse protéomique et des tests de proximité utilisant des anticorps spécifiques aux sous-unités. Elles soutiennent même que la plupart des récepteurs GABAB se trouvent effectivement dans une organisation quaternaire multimérique dans les cellules natives. Grâce à la collaboration entre l’équipe « Neurorécepteurs, dynamique et fonctions » animée par Philippe Rondard à l’IGF, le laboratoire de Jianfeng Liu à Wuhan (Chine) et celui de Yan Zhang à Hangzhou (Chine), la structure par cryo-microscopie électronique du tétramère GABAB a été élucidée. Cette structure confirme en grande partie les données précédentes et illustre comment une sous-unité GABAB1 empêche la liaison du ligand sur la sous-unité associée, par le biais d’une interaction de liaison asymétrique entre les domaines de liaison de GABAB1. Bien qu’une telle allostérie négative entre les hétérodimères au sein de ces complexes remette en question leur pertinence physiologique, certaines variantes génétiques associées à des maladies humaines affectent principalement la fonction des tétramères, plutôt que celle des hétérodimères, soulignant les premiers comme des acteurs importants pour les fonctions cérébrales normales7.
Ces découvertes ouvrent de nombreuses perspectives nouvelles pour réguler avec précision l’activité des récepteurs GABAB dans le cerveau et soulignent encore davantage le caractère unique de ce récepteur.
Ce travail vient d’être publié dans la revue Nature Communications.
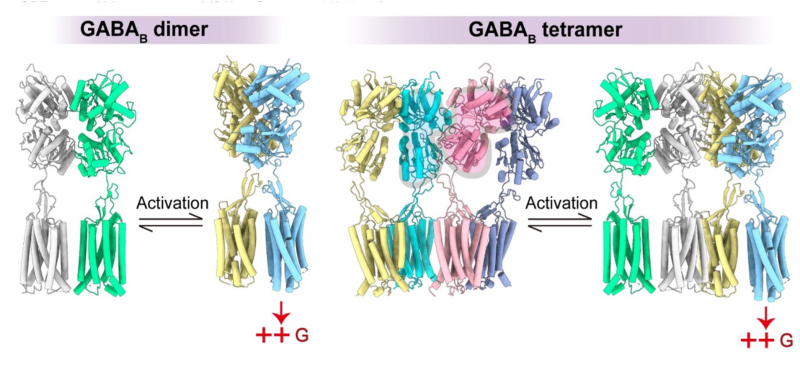
Mode d’activation différent des récepteurs GABAB dimériques et tétramériques. Dans le cas du dimère, la liaison du GABA dans la sous-unité GB1 (grise), conduit à la fermeture du VFT (jaune), et au mouvement relatif des deux sous-unités l’une par rapport à l’autre, conduisant à l’activation du domaine membranaire de GB2 (bleu), qui peut alors activer une protéine G. Dans le cas du tétramère, l’association asymétrique des deux sous-unités GB1 (bleu et rose), conduit à la fermeture d’un seul GB1 (jaune), et en conséquence à l’activation d’un seul GB2 (bleu). Mais quel peut être l’intérêt d’un tel système d’un point de vue physiologique ? Nous n’avons pas la réponse à cette question, mais nous pouvons spéculer que le deuxième récepteur, au sein du tétramère, offre la possibilité à des protéines d’interaction d’agir, et éventuellement d’activer d’autres voies de signalisation.


