Équipe Philippe MARIN
Neuroprotéomique et signalisation des pathologies cérébrales
Projet Communication neurone-glie au cours de la dégénérescence développementale et pathologique
RESPONSABLE

Personnel IGF impliqué
Marie-Laure PARMENTIER
DR2 Inserm
Julien VILLENEUVE
CRCN CNRS
Charline GAL
Doctorante CNRS
Camille ENJOLRAS
IE CDD CNRS

Le système nerveux est initialement surpeuplé de neurones. S’ensuit une période clé de remodelage, au cours de laquelle un sous-ensemble de connexions inappropriées est supprimé. L’élimination neuronale est également nécessaire après une lésion du système nerveux. Dans les deux cas, l’élimination des débris résultants est principalement assurée par la glie phagocytaire. Par conséquent, la sélection de connexions spécifiques pour l’élimination implique une communication essentielle entre les neurones et la glie. La signalisation via des chimiokines est fondamentale pour guider les réponses gliales. Cependant, la manière dont les chimiokines assurent la communication entre les neurones et la glie phagocytaire est actuellement peu connue.
Nous avons récemment identifié chez la drosophile une molécule de type chimiokine que nous avons nommée Orion. Orion joue un rôle majeur dans le remodelage du système nerveux de la drosophile, tant au cours du développement que des lésions, assurant la communication neurone-glie dans plusieurs types de neurones en dégénérescence. Orion est nécessaire à l’infiltration gliale dans les faisceaux axonaux et à la phagocytose des débris axonaux restants. Pour comprendre ces mécanismes, nos recherches poursuivent les trois objectifs suivants :
- Caractériser l’organisation topologique d’Orion lors de sa libération
La façon dont Orion est présenté par les neurones pourrait-elle être le facteur déterminant dans la modulation de l’activation des récepteurs gliaux et des réponses gliales intracellulaires ultérieures conduisant à l’infiltration des faisceaux axonaux ou à la phagocytose ? Nous nous concentrons sur la façon dont les neurones présentent Orion à la glie. Notre objectif est de déterminer dans quelle mesure un mode particulier de présentation d’Orion – Orion lié aux glycosaminoglycanes au niveau de la membrane plasmique neuronale par rapport à Orion « libre » ou transporté par des vésicules extracellulaires (VE) – conduit à des comportements gliaux spécifiques.
- Décrypter des voies de signalisation gliales activées par différentes formes d’Orion
L’infiltration, l’engloutissement et la phagocytose sont des mécanismes concomitants difficiles à dissocier, car la glie phagocyte les neurones tout en infiltrant progressivement les faisceaux axonaux. Nous cherchons à déterminer le rôle d’Orion dans la formation et la maturation des phagosomes gliaux grâce à des approches de génétique de la drosophile et de biologie cellulaire. De plus, nous combinerons le séquençage d’ARN en masse et en cellule unique dans des astrocytes de drosophile issus de différents contextes génétiques d’Orion, ce qui nous permettra de bloquer sélectivement l’infiltration gliale, la phagocytose ou les deux, et de comparer ces résultats à ceux de type sauvage. Cela révélera les signatures moléculaires et les réseaux de régulation spécifiquement impliqués dans chacun de ces mécanismes.
- Déterminer l’implication gliale dans la dissémination de Tau et d’APP lors de la phagocytose médiée par Orion
La maladie d’Alzheimer est caractérisée par l’accumulation d’agrégats intracytoplasmiques de la protéine Tau, une protéine de liaison aux microtubules, ainsi que par la formation de plaques amyloïdes extracellulaires. On pense que la protéine Tau se propage à la manière d’un prion entre des régions cérébrales interconnectées. Cependant, les mécanismes de sécrétion et de dissémination de Tau en conditions physiologiques et pathologiques restent flous. Notre objectif est de comprendre le rôle de la glie phagocytaire, activée par Orion, dans la dissémination des agrégats de Tau / Aß42 au cours du développement et du vieillissement cérébraux.
Nous utilisons des approches génétiques chez la drosophile (ex : analyse mosaïque avec induction de clones MARCM, systèmes d’expression génique binaire…), ainsi que des techniques de biochimie (isolement de l’hémolymphe et des VE), de biologie cellulaire et de microscopie à haute résolution.
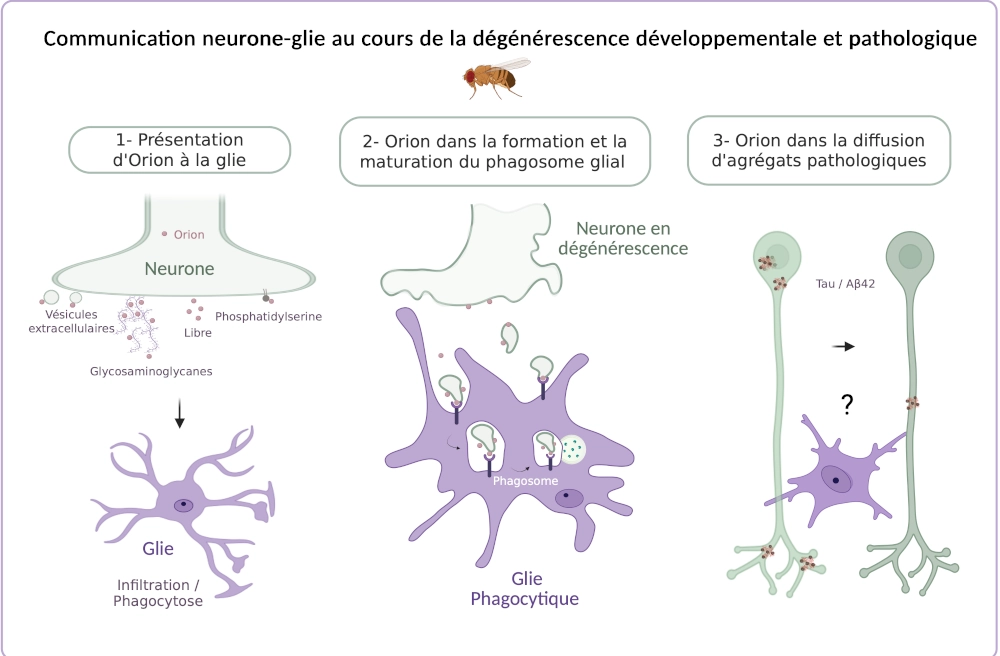
Orion, un signal de type chimiokine, marque les neurones en dégénérescence pour la phagocytose gliale. Le rôle d’Orion dans la propagation des agrégats de Tau / Aß42 sera étudié lors de la phagocytose gliale.
Principales publications
• Gal C., et al (2025) Cell signal, 3, 135.
• Perron C., et al. (2023) Development, 150, dev201633.
• Ji H., et al (2023) Proc Natl Acad Sci USA, 120, e2303392120.
• Boulanger A. and Dura J-M. (2022) Bioessays, 44, e2100254.
• Boulanger A., et al (2021) Nature Commun, 23, 1849.
• Boulanger A., et al (2012) PLoS ONE, 7, e40255.
• Boulanger A., et al (2011) Nature Neurosci, 14, 37.
Financements
• 2024-2028 ANR 2024-ExORION – Coordinateur
• 2022-2025 ANR 2024-ORIO – Responsable scientifique
• 2006-2007 AFM
• 2003-2005 Marie-Curie EU individual and experienced researcher fellowship
• 2002-2003 FRM
Collaborations
• Jean Maurice Dura (France)
• Hugues Lortat-Jacob (France)
• Lukas Neukomm (Suisse)
• Chun Han (USA)
• Lee Fradkin (USA)
Alumni
• Clarisse Perron (IE, 2022-2025)
• Ouidi Fatima Ezzahara (M2, 2025)
• Charline Gal (M2, 2024)
• Salomé Ruiz-Demoulin (M1, 2021)
• Héloïse Szczkowski (M2, 2020)
• Camille Thinat (IE, 2016-2019)


