Depuis près de 20 ans, il est proposé que l’activité des récepteurs membranaires peut être régulée par d’autres récepteurs qui, via une interaction directe, vont stabiliser une conformation active ou inactive de leur cible. Cette hypothèse offre la possibilité aux cellules d’intégrer les signaux externes qui viennent agir sur la multitude de récepteurs à leur surface. Bien que séduisante, cette hypothèse a été souvent remise en cause, et en tout cas, jamais clairement illustrée.
Au travers d’une collaboration entre les équipes de Philippe Rondard à l’IGF, de Jianfeng Liu à Wuhan, et de Jesús Giraldo à Barcelona, il vient d’être montré comment un récepteur de classe A peut stabiliser dans sa forme active le récepteur mGlu2 du glutamate.
Le récepteur mGlu2 est un récepteur dimérique constitutif où la liaison du glutamate entraine un mouvement relatif important entre les deux sous-unités. Ce mouvement est tel que l’interface de contact au niveau des domaines membranaires est totalement différente entre la forme inactive (qui implique les hélices transmembranaires 3 et 4), et la forme active (qui implique les hélices transmembranaires 6). Les auteurs montrent qu’en interagissant sélectivement avec l’interface 3-4 du récepteur mGlu2 inaccessible quand le récepteur est inactif, le récepteur de la sérotonine 5HT2a, stabilise le récepteur mGlu2 dans sa forme active. Ces résultats, basés sur des approches complémentaires de biochimie et sur l’utilisation de différents biosenseurs, démontrent qu’un récepteur membranaire peut agir comme un modulateur allostérique positif d’un récepteur mGlu. Les auteurs identifient par ailleurs plusieurs récepteurs capables de contrôler ainsi l’activité de mGlu2.
Sachant que les récepteurs mGlu2, ainsi que 5HT2a sont des cibles d’antipsychotiques, mieux comprendre leur interaction fonctionnelle peut ouvrir des voies pour mieux agir sur la schizophrénie.
D’autres récepteurs mGlu, comme mGlu5, sont aussi reconnus comme la cible de récepteurs couplés aux protéines G, comme les récepteurs de la dopamine ou de l’adénosine. Un mécanisme de régulation similaire est fort probable, comme déjà illustré au travers d’un travail réalisé en collaboration avec l’équipe de Julie Perroy à l’IGF (Sebastianutto et al., J Clin Invest, 2020), montrant l’importance d’un tel phénomène dans la maladie de Parkinson.
Ce travail vient d’être publié dans la revue Nature Communications.
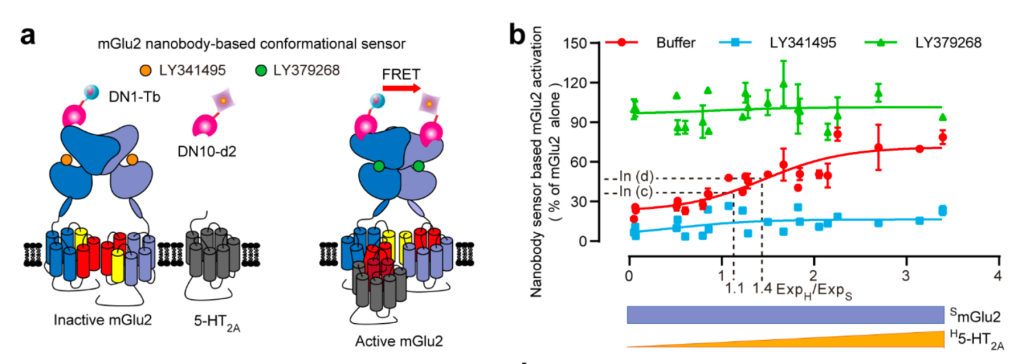
Le récepteur de la sérotonine 5HT2a, en interagissant spécifiquement avec la forme active du récepteur mGlu2, est capable de le stabiliser dans sa forme active. a) Schéma illustrant l’interaction du récepteur 5HT2a avec les hélices transmembranaires des sous-unités de mGlu2 disponibles uniquement quand le récepteur est actif (en rouge). La forme active du récepteur est détectée à l’aide de deux nanocorps, dont l’un ne se fixe que sur la forme active, seule situation générant un signal de transfert d’énergie de type FRET. b) Evolution de la proportion de récepteurs mGlu2 sous forme active détectés à l’aide des deux nanocorps en présence de quantité croissante du récepteur 5HT2a. En présence de l’agoniste de mGlu2 (en vert), les récepteurs sont toujours dans leur forme active (FRET élevé), alors qu’en présence d’antagoniste, (en bleu), les récepteurs restent dans leur forme inactive (faible FRET). En absence de ligand de mGlu2, on constate que la proportion de récepteur actifs augmente avec la quantité de récepteurs 5HT2a.


