Thème de recherche
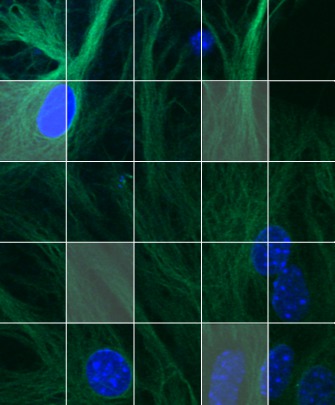
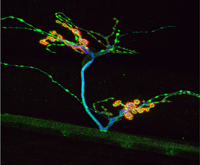
L’équipe a deux axes de recherche majeurs: l’un consiste à étudier les mécanismes normaux du fonctionnement du système nerveux, en utilisant majoritairement, pour ses propriétés génétiques remarquables, le modèle animal Drosophile (ou mouche du vinaigre). L’utilisation de ce modèle a aussi pour avantage de limiter l’utilisation de modèles animaux comme la souris ou le rat, suivant ainsi la directive européenne des « 3R » (remplacer, réduire et perfectionner l’utilisation des animaux en Europe) et les préconisations du comité d’éthique national sur l’expérimentation animale. Dans ce cadre, les projets développés consistent à comprendre le rôle des microtubules, des modifications post-traductionnelles qu’ils subissent, ainsi que le rôle des protéines qui y sont associées (ou MAPs pour microtubule-associated proteins), notamment au niveau de la morphologie et de la physiologie des axones et des synapses.
Le deuxième axe de recherche consiste à mieux comprendre les mécanismes physiopathologiques mis en jeu lors de maladies neurodégénératives comme la maladie de Huntington ou les tauopathies, en privilégiant comme modèle animal.
Ainsi, pour la maladie de Huntington, nous avons montré que la protéine sauvage (normale) Huntingtine jouait un rôle protecteur par rapport à la protéine mutée dans la maladie (qui comporte un domaine polyQ) et nous avons trouvé, en suivant cette hypothèse, un peptide capable d’améliorer nombre de déficits cellulaires, physiologiques et comportementaux induits par la protéine mutée (brevet déposé).
Nous travaillons maintenant sur la toxicité de la protéine associée aux microtubules, Tau. Cette protéine est fortement hyperphosphorylée et peut former des fibrilles dans la maladie d’Alzheimer et d’autres tauopathies (Démences fronto-temporales, maladie de Pick, Dégénérescence cortico-basale...) . Ce travail a débuté, via un financement de l’association France Alzheimer, puis dans le cadre du projet Diatral (DIAgnostic et TRaitement de la maladie d’Alzheimer) et a permis de montrer à quel point un excès de Tau sur les microtubules était en fait bien plus toxique qu’un excès de Tau hyperphosphorylé (localisé en dehors des microtubules) (Talmat-Amar et al, Human Molecular Genetics 2011). Ceci amène à reconsidérer certaines stratégies thérapeutiques employées pour traiter la maladie d’Alzheimer (voire les autres tauopathies) qui consistent à déphosphoryler Tau. Nous recherchons actuellement de nouvelles stratégies de contrôle de la fixation de Tau aux microtubules, indépendantes de la régulation de la phosphorylation, afin d’imaginer des stratégies thérapeutiques innovantes. Nous avons aussi récemment montré qu’un excès de Tau bloquait la division cellulaire (Bougé et al. 2016), ce qui ouvre des perspectives nouvelles tant dans la recherche des dysfonctionnements liés à Tau en dehors du système nerveux que dans la compréhension des dysfonctionnements du système nerveux dès la division des cellules souches et non plus seulement au niveau des neurones différenciés.