GÉNOMIQUE FONCTIONNELLE DES GÈNES SOUMIS À EMPREINTE PARENTALE
Département : Physiologie et Cancer
Thème de recherche
Pour plus d'informations, visitez le Site de l'équipe.
Notre équipe combine biologie moléculaire, biologie cellulaire (en particulier des cellules souches), génomique et statistiques pour identifier les fonctions des gènes soumis à empreinte génomique parentale.
L'empreinte génomique parentale est un mécanisme épigénétique qui limite l'expression de certains gènes à un seul de leur 2 allèles en fonction de son origine parentale. L'empreinte génomique est essentielle au développement embryonnaire et affecte environ 150 gènes chez les mammifères placentaires (euthériens) et une dizaine chez les marsupiaux (metathériens). Ce mécanisme n'a pas été observé chez les mammifères ovipares (protothériens) et les autres clades (oiseaux, reptiles, amphibiens, poissons...)
Chez l'Homme, des défauts d'empreinte sont responsables de différents syndromes présentant des phénotypes complexes: Syndromes de Silver-Russel, Angelman, Prader-Willi, Beckwith-Wiedemann, Temple, Kagami-Ogata, pseudohypoparathyroïdisme et diabètes néonatal transitoire. Certains gènes soumis à empreinte sont également impliqués dans la formation de tumeurs comme oncogène ou gène suppresseur de tumeurs.
Nous avons montré que les gènes soumis à empreinte font partie d'un réseau de gènes co-régulés que nous avons appelé le "réseau des gènes soumis à empreinte" (IGN; Varrault et al., Dev. Cell, 2006). Nous avons ensuite démontré que l'IGN était régulé lorsque des cellules quittent le cycle cellulaire et entrent en quiescence ou se différencient. C'est en particulier le cas in vitro pour des fibroblastes primaires ou des préadipocytes et in vivo lors de la régénération musculaire. L'IGN comprend également des gènes d'expression biallélique, en particulier des gènes qui contrôlent la composition de la matrice extracellulaire. Ces observations suggèrent que les gènes soumis à empreinte sont impliqués dans un processus biologique commun qui sous-tend leur impact sur le développement embryonnaire, l'obésité, le diabètes, la physiologie musculaire et la formation de tumeurs (Al Adhami et al., Genome Res., 2015).
Nous poursuivons l'étude de la fonction des gènes soumis à empreinte en utilisant différents systèmes biologiques et en combinant des approches pan-génomiques.
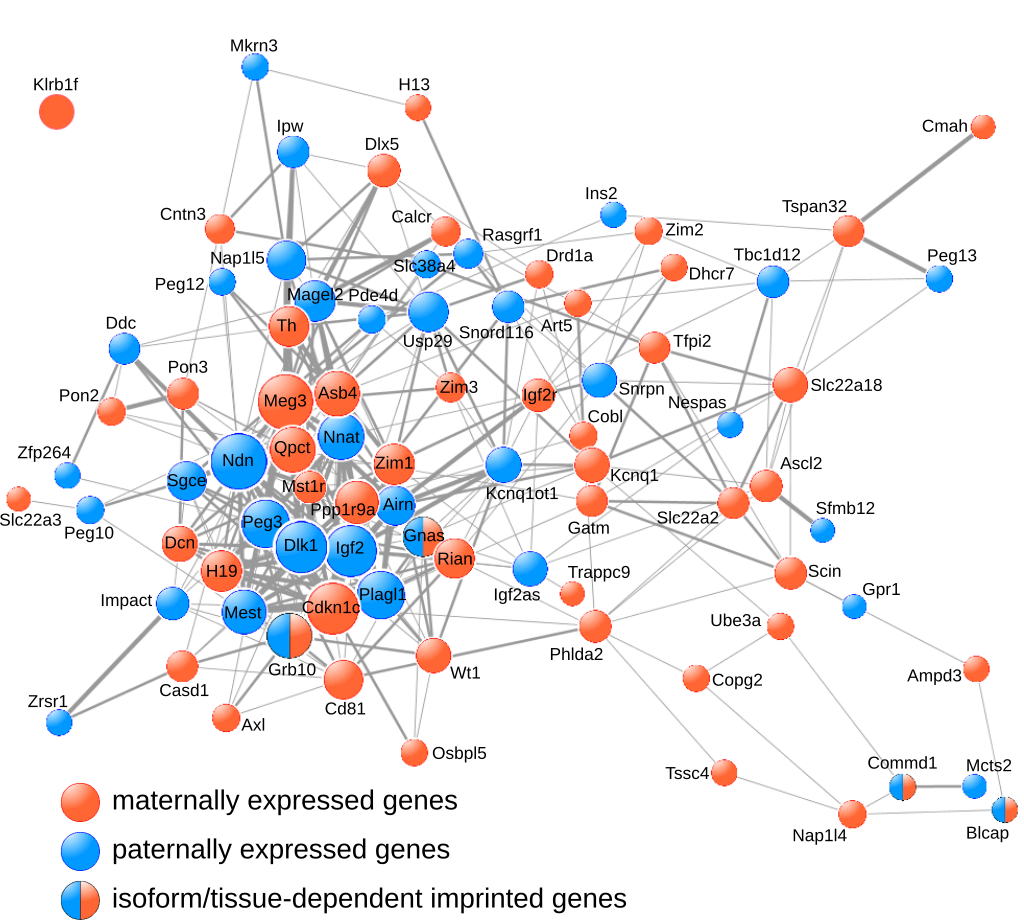
Les gènes soumis à empreinte sont fréquemment coexprimés.
La coexpression des gènes soumis à empreinte mruins a été mesurée en utilisant la méta-analyse de données d'expression COXPRESdb.
Les liens de coexpression ont été représentés en utilisant Cytoscape. La taille des sommets est proportionnelle à la connectivité du sommet et l'épaisseur des arrêtes représente le rang mutuel entre 2 sommets.
Publications majeures
- Reynès C, Kister G, Rohmer M, Bouschet T, Varrault A, Dubois E, Rialle S, Journot L, Sabatier R (2019) ISoLDE: a data-driven statistical method for the inference of allelic imbalance in datasets with reciprocal crosses. Bioinformatics. pii: btz564. doi: 10.1093/bioinformatics/btz564.
- Baudement MO, Cournac A, Court F, Seveno M, Parrinello H, Reynes C, Sabatier R, Bouschet T, Yi Z, Sallis S, Tancelin M, Rebouissou C, Cathala G, Lesne A, Mozziconacci J*, Journot L*, Forné T* (2018) High-salt-recovered sequences are associated with the active chromosomal compartment and with large ribonucleoprotein complexes including nuclear bodies. Genome Res. 28:1733-1746. doi: 10.1101/gr.237073.118.
- Varrault A, Dantec C, Le Digarcher A, Chotard L, Bilanges B, Parrinello H, Dubois E, Rialle S, Severac D, Bouschet T, Journot L (2017) Identification of Plagl1/Zac1 binding sites and target genes establishes its role in the regulation of extracellular matrix genes and the imprinted gene network. Nucleic Acids Res. 45:10466-10480. doi: 10.1093/nar/gkx672.
- Bouschet T, Dubois E, Reynès C, Kota SK, Rialle S, Maupetit-Méhouas S, Pezet M, Le Digarcher A, Nidelet S, Demolombe V, Cavelier P, Meusnier C, Maurizy C, Sabatier R, Feil R, Arnaud P, Journot L, Varrault A (2017) In Vitro Corticogenesis from Embryonic Stem Cells Recapitulates the In Vivo Epigenetic Control of Imprinted Gene Expression. Cereb Cortex. 27:2418-2433. doi: 10.1093/cercor/bhw102.
- Al Adhami H, Evano B, Le Digarcher A, Gueydan C, Dubois E, Parrinello H, Dantec C, Bouschet T, Varrault A, Journot L (2015) A systems-level approach to parental genomic imprinting: the imprinted gene network includes extracellular matrix genes and regulates cell cycle exit and differentiation. Genome Res. 25:353-67. doi: 10.1101/gr.175919.114.