MUTATIONS GAIN DE FONCTION D’UN CANAL CALCIQUE : UNE CAUSE AVÉRÉE DE L’ATROPHIE CÉRÉBELLEUSE DE L’ENFANT
Des chercheurs de l’institut des maladies génétiques Imagine de Paris - l’équipe de Vincent Cantagrel - et de l’Institut de Génomique Fonctionnelle de Montpellier - l’équipe de Philippe Lory - se sont associés pour identifier et caractériser des gènes responsables de l’atrophie cérébelleuse de l’enfant. Cette étude publiée le 5 juin dans la revue Brain identifie comme mécanisme causal de cette pathologie, l’activité exacerbée d’un canal calcique de type T.
Le cervelet est impliqué dans la gestion de l’équilibre et la coordination des mouvements. Ce ‘petit cerveau’ joue également un rôle clé dans l’apprentissage chez l’enfant. Les pathologies du cervelet sont multiples, avec en particulier différentes forme d’ataxies et de troubles cognitifs, et il apparait que le développement incorrect du cervelet est très souvent responsable de ces maladies. Ces pathologies congénitales du cervelet sont souvent associées à des anomalies visibles à l’imagerie telle que l’atrophie cérébelleuse et dont les causes sont encore mal connues.
Les généticiens parisiens ont criblé une cohorte de 47 patients et identifiés que 35 % d’entre eux présentaient des mutations de novo, c’est-à-dire non héritées. Parmi ces gènes mutés responsables des formes pédiatriques d’atrophie cérébelleuse, beaucoup d’entre eux pointent sur un défaut d’homéostasie et de signalisation calcique. L’étude de quatre patients présentant des mutations de novo dans le gène CACNA1G a permis de définir une nouvelle canalopathie caractérisée par une encéphalopathie très sévère et résultant de mutations potentiellement activatrices. Pour tester cette hypothèse, les électrophysiologistes montpelliérains ont étudié les conséquences fonctionnelles des mutations du gène CACNA1G qui code pour un canal calcique de type T (Cav3.1) exprimé très fortement et très précocement dans le cervelet.
Les données fonctionnelles sont sans appel : les deux mutations, dont celle retrouvée chez trois patients, provoquent une augmentation significative d’activité du canal calcique. En modélisant l’activité des neurones des noyaux profonds du cervelet, ils identifient également une augmentation de l’excitabilité de ces neurones. Puisqu’il existe des inhibiteurs assez sélectifs de ces canaux, les chercheurs les ont utilisé pour montrer qu’il était possible de corriger l’activité aberrante des canaux mutés. Cette étude améliore la compréhension des bases génétiques de l’atrophie cérébelleuse de l’enfant et propose, grâce à l’identification d’un mécanisme causal impliquant un défaut de signalisation calcique, une piste thérapeutique qui pourrait être rapidement évaluée.
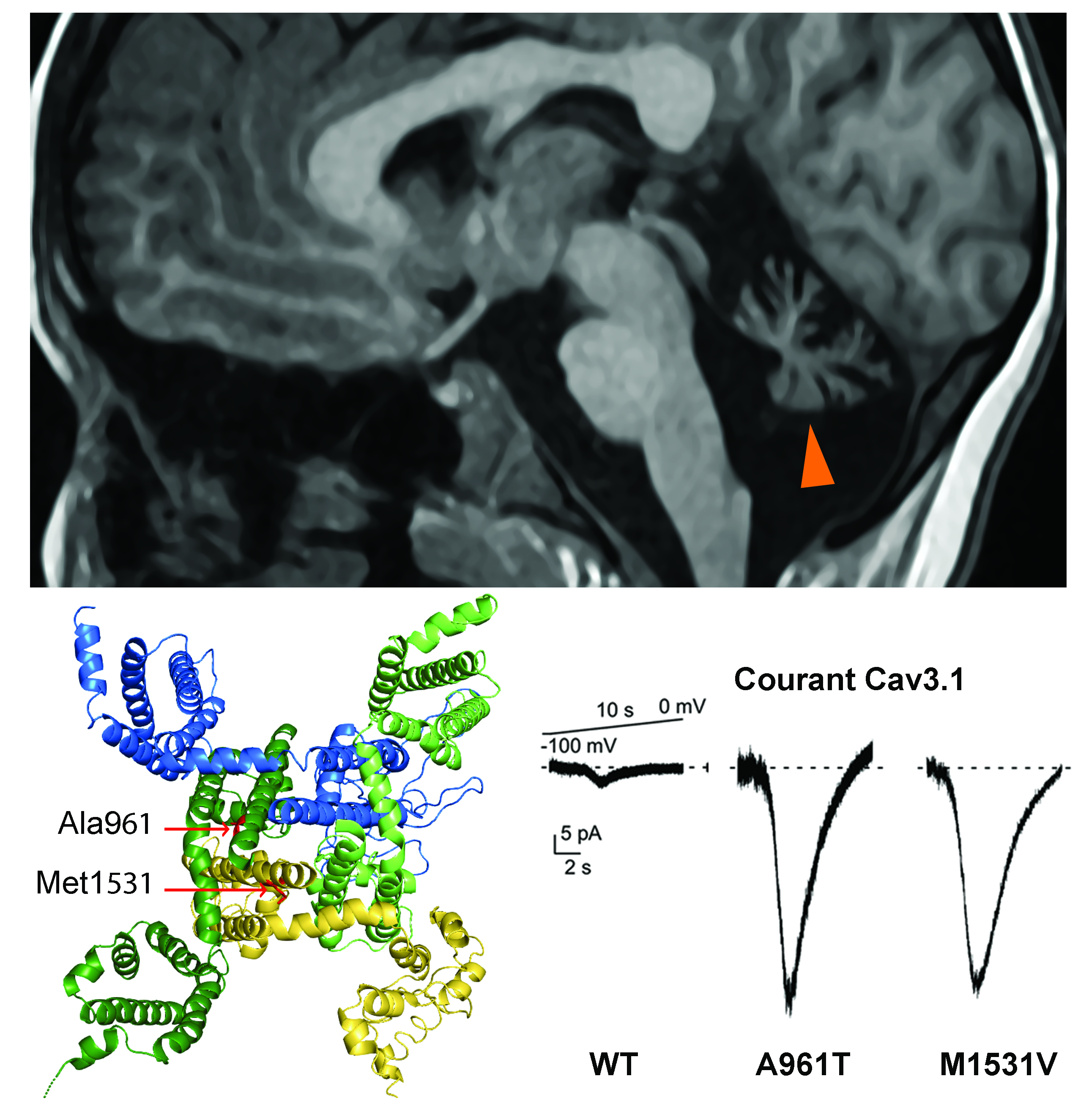
Des mutations de novo du gène CACNA1G sont responsables d’une encéphalopathie avec atrophie cérébelleuse (flèche orange) entrainant des troubles sévères du développement moteur et cognitif.
Ces mutations (A961T et M1531V) sont localisées au niveau du pore du canal calcique Cav3.1 codé par le gène CACNA1G et entrainent une augmentation importante de l’activité du canal (courant Cav3.1).
LIEN PUBLICATION / PUBLICATION LINK
Référence article :
Chemin J, Siquier-Pernet K, Nicouleau M, Barcia G, Ahmad A, Medina-Cano D, Hanein S, Altin N, Hubert L, Bole-Feysot C, Fourage C, Nitschké P, Thevenon J, Rio M, Blanc P, Vidal C, Bahi-Buisson N, Desguerre I, Munnich A, Lyonnet S, Boddaert N, Fassi E, Shinawi M, Zimmerman H, Amiel J, Faivre L, Colleaux L, Lory P, Cantagrel V. De novo mutation screening in childhood-onset cerebellar atrophy identifies gain-of-function mutations in the CACNA1G calcium channel gene. Brain. 2018 Jun 5. doi: 10.1093/brain/awy145. [Epub ahead of print] PubMed PMID: 29878067.
DE NOVO ‘GAIN OF FUNCTION’ MUTATIONS IN T-TYPE CALCIUM CHANNELS : A PRIMARY CAUSE OF CHILDHOOD CEREBELLAR ATROPHY
The group of Philippe Lory at IGF has teamed up with the group of Vincent Cantagrel at Imagine Institute for Genetic Diseases of Paris to identify and characterize genes responsible for cerebellar atrophy in children. This study, just published in Brain (PMID : 29878067), identifies as a causal mechanism of this pathology, the exacerbated activity of a T-type calcium channel Cav3.1.
The cerebellum is involved in the motor coordination and skilled movements. It also plays a key role in learning. There is a wide range of diseases related to cerebellum dysfunction, including various forms of ataxia and cognitive disorders. An incorrect development of the cerebellum is often responsible for the congenital forms of these diseases. Cerebellar atrophy, which can be observed using MRI, is often associated with early-onset cerebellar diseases.
Geneticists in Paris have screened a cohort of 47 patients with cerebellar atrophy and identified that 35% had de novo mutations. Among these mutated genes responsible for pediatric forms of cerebellar atrophy, many of them point to potential defects in calcium homeostasis or calcium signaling. The study of four patients with de novo mutations in the CACNA1G gene led to the definition of a new channelopathy characterized by very severe encephalopathy. To test this hypothesis, electrophysiologists in Montpellier have studied the functional consequences of 2 mutations in the CACNA1G gene, which codes for a T-type calcium channel (Cav3.1) expressed very strongly and very early in the cerebellum.
These two mutations, especially the one found in three patients, cause a significant increase in calcium channel activity. By modeling the activity of neurons of the deep nuclei of the cerebellum, an increase in the excitability of these neurons was identified. The use of selective inhibitors of T-type calcium channels showed that the aberrant activity of the mutant channels can be corrected. This study improves our understanding of the genetic basis of childhood cerebellar atrophy and proposes, through the identification of a causal mechanism involving a gain of T-type channel activity, a therapeutic option that could be quickly evaluated.